随着免疫细胞疗法逐渐进入大众视野,越来越多的细胞治疗产品涌现市场,它们的种类繁多,究竟该如何选择?本文将为您详细解析市面上常见的免疫细胞疗法,力求为您提供最为中肯和准确的建议。
一、核心免疫细胞疗法对比
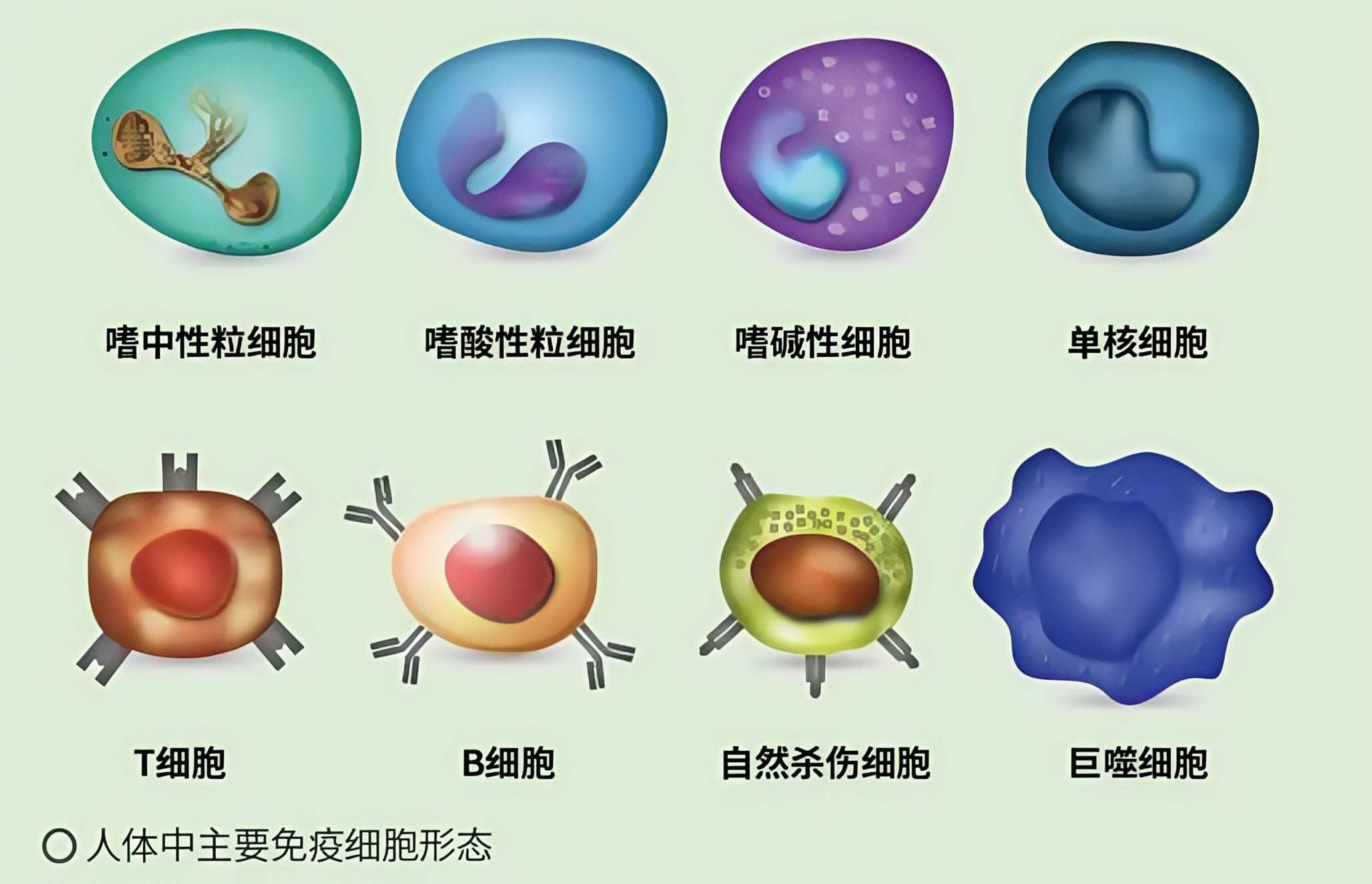
市面上的主流免疫细胞疗法,除了大家耳熟能详的CAR-T细胞外,还有NK细胞、T细胞等。每一种细胞都有各自的优点与不足,具体来说区别如下:
1.NK细胞:免疫系统的“先锋部队
NK(自然杀伤细胞)属于先天性免疫细胞,无需抗原预先致敏即可快速反应并非特异性产生杀伤效果。与其他免疫细胞不同,NK细胞单独就能识别和攻击外来细胞、癌细胞和病毒,其作用特点如下:
- 优势:起效快、安全性高,无移植物抗宿主病(GVHD)风险,适合健康人群的免疫保养(如抗衰老、预防感染)。
- 局限:缺乏免疫记忆功能,对实体瘤的长期控制较弱,需定期回输。
- 适用场景:具有强大的杀伤与免疫调节能力。可用于恶性血液病(如白血病)、黏膜相关性肿瘤,或作为联合治疗的辅助手段。

2. T细胞:精准打击的“特种兵”
T细胞属于适应性免疫,需抗原激活后分化为细胞毒性T细胞(CTL)或辅助T细胞。CAR-T和TCR-T是基因改造后的T细胞,可特异性识别癌细胞。
- CAR-T的突破:针对CD19等靶点,在血液瘤(如淋巴瘤)中疗效显著,但价格高昂(约120万元/针),且可能引发细胞因子风暴。
- 局限:实体瘤因靶点异质性和免疫抑制微环境,CAR-T疗效受限。传统T细胞依赖MHC分子,易被癌细胞逃逸。
3.CIK细胞:广谱抗癌的“机械化步兵”
CIK(细胞因子诱导杀伤细胞)由外周血单个核细胞经细胞因子(如IL-2、IFN-γ)刺激生成,兼具T细胞活性与NK细胞的非MHC限制性,也被称为“NKT样细胞”。
- 优势:增殖速度快(体外扩增50倍以上)、杀瘤谱广,尤其对胃癌、乳腺癌等实体瘤效果显著,无需进行基因改造,扩增周期较短(约2周时间)。
- 联合治疗:常与DC细胞联用(DC-CIK),通过抗原呈递增强靶向性,在肝癌、肺癌中表现优异。
- 成本优势:单次治疗费用和性价比优于CAR-T细胞。
二、其他常见免疫细胞
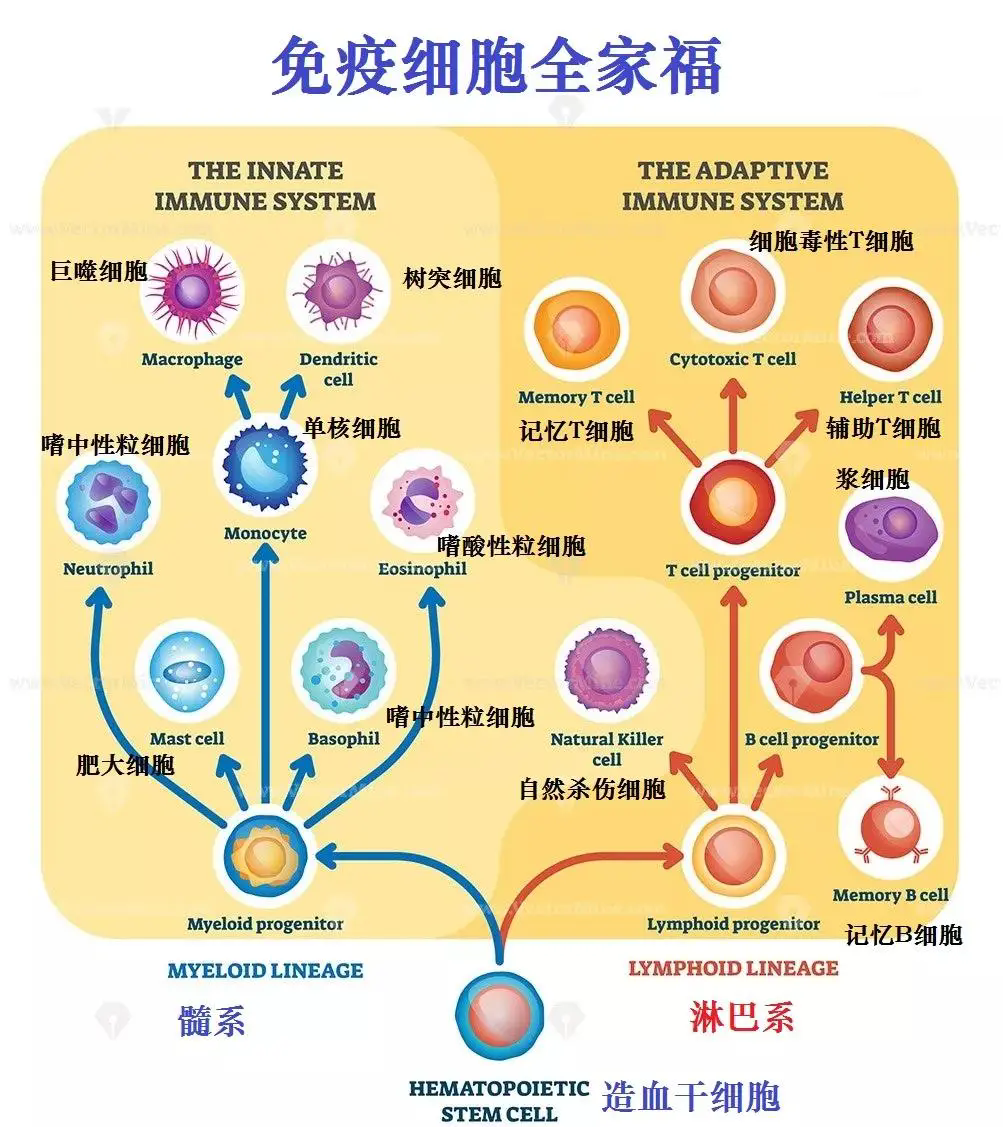
1.DC细胞:免疫应答的“指挥官”
树突状细胞(DC)是抗原呈递的核心,能将肿瘤抗原信息传递给T细胞,激活特异性免疫。
- 优势:安全性高,非毒性 。
- 局限:而体外负载抗原,制备流程复杂。且单独使用杀伤力较弱,常与CIK/NK联合使用。
- 应用:目前主要在黑色素瘤、前列腺癌等中作为疫苗接种研究。
2.γδT细胞:肿瘤干细胞的“清道夫”
γδT细胞表达特异性γδTCR和NK受体,介于先天与适应性免疫之间,能识别应激抗原(如磷酸抗原),对肿瘤干细胞具有强杀伤力,具有双重杀伤机制和MHC非限制性特性。
- 优势:可识别多种肿瘤抗原且低GvHD风险。
- 局限:体外扩增技术尚在完善中,临床规模化面临挑战。
- 临床试验:已在急性髓系白血病等进行I期研究。
4.TIL细胞:实体瘤的革命突破
TIL(Tumor-Infiltrating Lymphocyte)细胞疗法疗法利用患者肿瘤组织中筛选的效应淋巴细胞,体外大规模扩增后回输,针对实体瘤展现特异性杀伤
- 优势:对黑色素瘤等实体瘤缓解率可达50%以上。
- 局限:制备流程耗时(月级)、成本高且需大肿瘤组织采样。
- 应用:国内外多项临床试验正在探索TIL在实体瘤中的效果。
三、选择策略:从个体化到联合治疗
1.根据癌症类型匹配
- 实体瘤:优先考虑CIK(尤其胃癌、乳腺癌)、DC-CIK(肝癌、肺癌)或γδT(肿瘤干细胞富集型)。
- 血液瘤:CAR-T(淋巴瘤、白血病)或NK细胞(恶性血液病)更具优势。
- 黑色素瘤/结肠癌:TIL(肿瘤浸润淋巴细胞)因高肿瘤特异性成为首选。
2.结合治疗阶段
- 术后辅助:CIK或NK清除残余癌细胞,降低复发风险。
- 晚期姑息治疗:联合方案(如DC-CIK+化疗)可延长生存期。
3.健康人群的预防:
4.成本与安全性考量:
- 经济受限者可选CIK或NK;
- 追求前沿技术且预算充足者可尝试CAR-T或γδT。
- 自体细胞安全性高于异体。
总结:
免疫细胞疗法的选择需综合癌症类型、分期、经济状况及个体差异,不存在“万能方案”。建议患者与主治医生及细胞治疗机构深入沟通,制定个性化方案。随着技术发展,更多联合疗法与新型细胞制剂(如CAR-γδT)或将颠覆传统抗癌格局,为患者带来新希望。